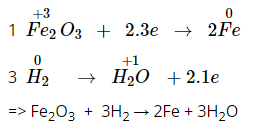1. Phản ứng oxi hóa – khử là gì?
Phản ứng oxi hóa – khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một nguyên tố hoặc phản ứng trong đó có sự chuyển electron giữa các chất phản ứng.
- Xác định số oxi hóa trong hợp chất: Người ta ghi số oxi hóa ở phía trên nguyên tử của nguyên tố, ghi dấu trước, số sau.
2. Quan hệ giữa hóa trị và số oxi hóa của nguyên tố
Hóa trị gắn liền với liên kết hóa học, số oxi hóa gắn liền với sự chuyển dịch electron nên nhiều khi số oxi hóa không trùng với hóa trị.
Các hợp chất của kim loại, giá trị tuyệt đối của số oxi hóa và hóa trị thường trùng nhau.
3. Chất khử, chất oxi hóa, sự oxi hóa và sự khử
Chất khử là chất nhường electron hay là chất có số oxi hóa tăng sau phản ứng.
Chất oxi hóa là chấ nhận electron hay chất có số oxi hóa giảm sau phản ứng.
Sự oxi hóa (quá trình oxi hóa) là quá trình làm cho chất đó nhường electron hay làm tăng số oxi hóa chất đó.
Sự khử (quá trình khử) của một chất là quá trình làm cho chất đó nhận electron hay giảm số oxi hóa của chất đó.
Chú ý: Sự oxi hóa và sự khử bao giờ cũng diễn ra đồng thời trong một phải ứng vì sự nhướng electron chỉ có thể xảy ra khi có sự nhận electron.
4. Lập phương trình phản ứng oxi hóa – khử
Bước 1: Ghi số oxi hóa của những nguyên tố có số oxi hóa thay đổi;
Ví dụ: ![]()
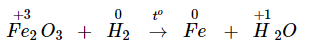
Bước 2: Viết phương trình oxi hóa và quá trình khử, cân bằng mỗi phương trình;
Ví dụ:
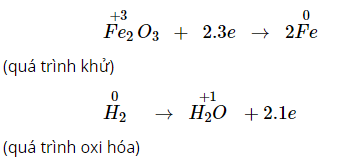
Bước 3: Tìm hệ số thích hợp sao cho tổng số electron do chất khử nhường bằng tổng số electron mà chất oxi hóa nhận.