
1, Khái niệm.
Ta được amin khi thay thế một hay nhiều nguyên tử hidro trong phân tử NH3 bằng một hay nhiều gốc hidrocacbon.
2, Danh pháp.
Danh pháp gốc-chức: Tên gốc hidrocacbon+amin.
VD: Metyl amin (CH3-NH2)
3, Phân loại:
- Theo đặc điểm cấu tạo của gốc hidrocacbon: amin thơm, amin béo, amin dị vòng.
- Theo bậc của amin: amin bậc một, amin bậc hai, amin bậc ba,…
Bậc của amin được tính theo số gốc hidrocacbon liên kết trực tiếp với nguyên tử N.
VD: Amin bậc 1 (CH3CH2CH2NH2); Amin bậc 2 (CH3CH2NHCH3); Amin bậc 3 ((CH3)3N).
4, Tính chất vật lí
Chất khí có mùi khai khó chịu, độc, dễ tan trong nước như: metyl, đimetyl; trimetyl; etylamin.
Những chất lỏng hoặc rắn, độ tan trong nước giảm dần theo chiều tăng của phân tử khối là các chất đồng đẳng cao hơn.
Anilin là chất không màu,lỏng, rất độc, ít tan trong nước, tan trong etanol, benzen.
5, Tính chất hóa học.
a, Phản ứng với axit nitro:
Ở nhiệt độ thường, amin bậc 1 tác dụng với axit nitro cho ancol hoặc phenol và giải phóng nito:
![]()
Ở nhiệt độ thấp, anilin và các amin thơm bậc một tác dụng với axit nitro cho muối điazoni: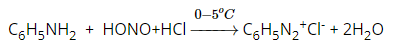
b, Tính bazo:
Amin tác dụng với axit tạo thành dung dịch muối:
RNH2 + HCl → RNH3Cl
Amin tác dụng với một số dung dịch muối có môi trường axit:
3RNH2 + FeCl3 + 3H2O -> Fe(OH)3 + 3RNH3Cl
c, Phản ứng ankyl hóa: RNH2 + R’I -> RNHR’ + HI
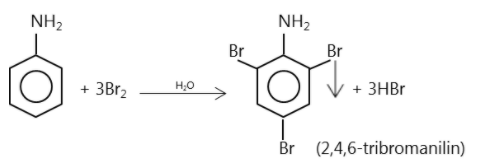
d, Phản ứng thế brom vào nhân thơm của anilin: tạo ra kết tủa trắng, dùng nhận biết anilin với các amin khác.
6, Ứng dụng:
- Tổng hợp hữu cơ, polime.
- Nguyên liệu quan trọng trong công nghiệp phẩm nhuộm, dược phẩm.
Hi vọng với bài viết này sẽ giúp ích cho các em trong quá trình học lớp 12.


























