Ở bài viết này, chúng ta sẽ cùng Thầy Vũ Khắc Ngọc (giáo viên môn Hóa học tại Hệ thống Giáo dục HOCMAI) đi tìm hiểu về Axit, bazơ và muối.
I. Axit.
a, Khái niệm.
Axit là chất trong nước phân li ra ion H+.
VD: HCl, H2SO4,CH3COOH.
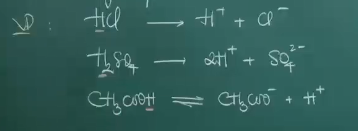
Axit nhiều nấc hay Axit nhiều lần axit là axit có nhiều H+.
VD: 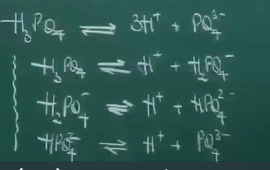
*Một số cation tương ứng với các bazo yếu cũng có tính axit: Al+,Fe+,NH4+,…
*Mọi dung dịch axit đều chứa ion H+ và các tính chất chung của dung dịch axit đều do ion H+ gây ra.
b, Tính chất:
- Đổi màu quỳ tím sang màu đỏ.
- Tác dụng với kim loại đứng trước Hidro tạo thành muối và H2.
- Tác dụng với bazo tạo thành muối và H2O.
- Tác dụng với oxit bazo tạo thành muối và H2O.
- Tác dụng với muối tạo thành muối mới và axit mới.
- Có vị chua.

II. Bazo.
Bazo là chất khi tan trong nước phân li ra ion OH-.
VD: 
*Chú ý: Trong thực tế một số bazo là phân tử không có nhóm OH: NH3,…
Một số anion gốc axit của axit yếu cũng có tính bazo.
Tính chất: Các dung dịch bazo đều có tính chất chung di ion OH- gây ra:
- Khả năng đổi màu chất chỉ thị: quỳ tím -> xanh, phenolphtalein -> hồng.
- Tác dụng với axit -> muối + nước.
- Tác dụng với oxit axit -> muối + nước.
- Tác dụng với muối tan -> muối mới+bazo mới.
III. Hidroxit lưỡng tính.
Hidroxit lưỡng tính là những hidroxit vừa có thể phân li theo kiểu bazo, vừa có thể phân li theo kiểu axit.
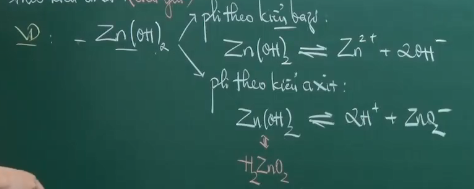
IV. Muối.
Muối là chất khi tan trong nước phân li ra cation kim loại hoặc amoni (NH4+) và anion gốc axit.
Hấu hết muối đều là chất điện li mạnh (phân li hoàn toàn trong nước).
Phân loại muối:
- Muối trung hòa là muối mà phân tử của nó không còn hidro mang tính axit.
- Muối axit là muối mà phân tử của nó còn hidro mang tính axit.
Hy vọng với bài viết này sẽ giúp ích cho các em trong quá trình học môn Hóa học lớp 11.


























