Ở bài viết này, chúng ta sẽ cùng Thầy Vũ Khắc Ngọc (giáo viên môn Hóa học tại Hệ thống Giáo dục HOCMAI) đi tìm hiểu về Phản ứng trao đổi trong dung dịch chất điện li.
I. Bản chất phản ứng của các chất trong dung dịch – phương trình ion thu gọn.
1. Bản chất phản ứng của các chất trong dung dịch.
*Bản chất phản ứng của các chất trong dung dịch là sự tương tác các ion với nhau.
VD: 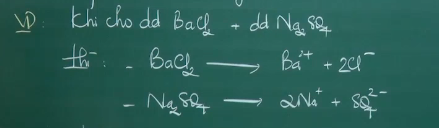
Phương trình ion thu gọn.
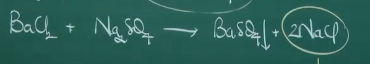
Bản chất: 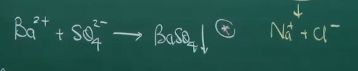
=> Phương trình trên gọi là phương trình ion thu gọn.
2. Cách viết phương trình ion thu gọn.
Bước 1: Viết phương trình phản ứng dạng phân tử.
Bước 2: Viết phương trình ion đầy đủ.
- Các chất vừa tan, vừa điện li mạnh -> Viết dưới dạng ion.
- Các chất rắn, khí, chất điện li yếu -> Viết dưới dạng phân tử.
Bước 3: Viết phương trình ion thu gọn bằng cách triệt tiêu các ion giống nhau.
VD: 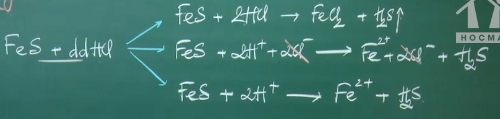
3. Đặc điểm ý nghĩa của phương trình ion.
- Thể hiện bản chất thực sự của phản ứng giữa các chất trong dung dịch, chỉ rõ những ion thực sự tham gia vào quá trình phản ứng.
- Cùng một phương trình ion thu gọn có thể tương ứng với nhiều phương trình phân tử khác nhau.
VD: Viết phương trình thu gọn của các phản ứng sau:
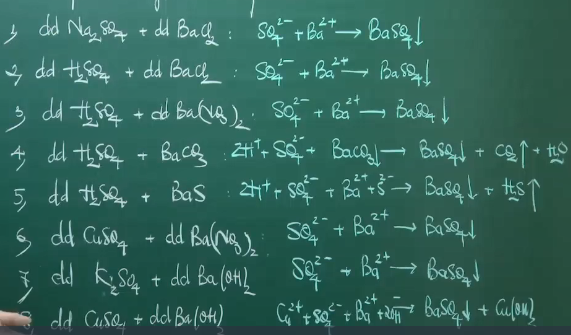
II. Phản ứng trao đổi ion trong dung dịch.
*Tổng quát: AB + DE -> AE + DB.
*Điều kiện để xảy ra phản ứng trao đổi ion:
- Đối với chất tha gia: phải tan (ngoại trừ phản ứng có axit tham gia).
- Đối với sản phẩm: Có ít nhất một chất tách ra khỏi dung dung dưới dạng kết tủa, chất khí, chất điện li yếu.
*Các trường hợp khác nhau của phản ứng trao đổi ion:
- Axit + bazo -> muối + nước.
- Axit + muối -> axit mới + muối mới.
- Muối tan + bazo tan -> bazo mới + muối mới.
- Muối tan + muối tan -> 2 muối mới.
Hy vọng với bài viết này sẽ giúp ích cho các em trong quá trình học môn Hóa học lớp 11.


























