I, Tinh thể nguyên tử
1. Tinh thể nguyên tử
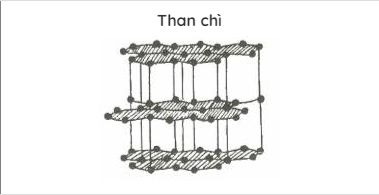
a, Tinh thể than chì
 Tính chất vật lý:
Tính chất vật lý:
- Tinh thể màu xám;
- Dẫn điện, dẫn nhiệt tốt;
- Mềm.
Cấu trúc:
- Cấu trúc lớp;
- Các lớp liên kết nhau bằng tương tác yếu.
Ứng dụng: Làm điện cực, làm nồi để nấu chảy hợp kim chịu nhiệt, chế tạo chất bôi trơn, bút chì đen.
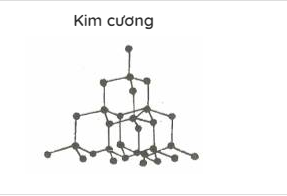
b, Kim cương
 Tính chất vật lý:
Tính chất vật lý:
- Tinh thể trong suốt, không màu;
- Không dẫn điện, dẫn nhiệt kém;
- Rất cứng, là chất cứng nhất trong tất cả các chất.
Cấu trúc:
- Tứ diện đều;
- Liên kết cộng hóa trị bền.
Ứng dụng:
Làm đồ trang sức, chế tạo mũi khoan, dao cắt thủy tinh, làm bột màu…
2. Tính chất chung của tinh thể nguyên tử
Lực liên kết cộng hóa trị trong tinh thể nguyên tử rất lớn, vì vậy tinh thể nguyên tử bền vững, rất cứng có nhiệt độ nóng chảy và nhiệt độ sôi khá cao.
Kim cương có độ cứng lớn nhất so với các tinh thể đã biết nên quy ước có độ cứng là 10 đơn vị. Đó là đơn vị đo độ cứng của các chất.
II, Tinh thể phân tử
1, Tinh thể phân tử
- Tại nút mạng, tinh thể là các phân tử iot;
- Các phân tử iot là tinh trong tinh thể hút nhau bằng lực tương tác yếu;
- Tinh thể iot là tinh thể phân tử, ở nhiệt độ thường iot ở thể rắn với cấu trúc tinh thể mạng lưới lập phương tâm diện, các phân tử iot ở 8 đỉnh và ở các tâ 6 mặt của hình lập phương.
2, Tính chất chung của tinh thể phân tử
- Trong tinh thể phân tử, các phân tử vẫn tồn tại những đơn vị độc lập và hút nhau bằng lực tương tác yếu giữa các phân tử. Vì thế, tinh thể phân tử dễ nóng chảy và bay hơi.
- Các tinh thể phân tử không phân cực dễ hòa tan trong các dung môi không phân cực như benzen, toluen, cacbon tetraclorua…



























