Đề cương ôn thi học kì 1 lớp 11 môn Hóa được HOCMAI biên soạn đầy đủ nội dung kiến thức lý thuyết cùng các dạng bài, bộ đề thi ôn luyện có hướng dẫn giải chi tiết. Các em học sinh hãy tham khảo kỹ để ôn tập cũng như chuẩn bị tốt nhất cho kỳ thi cuối HK1 sắp tới nhé!

⇒ Tham khảo thêm:
- Đề cương ôn thi học kì 1 môn Toán lớp 11
- Đề cương ôn thi học kì 1 môn Ngữ Văn lớp 11
- Đề cương ôn thi học kì 1 môn Lý lớp 11
- Đề cương ôn thi học kì 1 môn Sinh lớp 11
- Đề cương ôn thi học kì 1 Tiếng Anh lớp 11
A. KIẾN THỨC TRỌNG TÂM | ĐỀ CƯƠNG ÔN THI HỌC KÌ 1 MÔN HÓA 11
CHƯƠNG 1: SỰ ĐIỆN LI
1. Lý thuyết trọng tâm
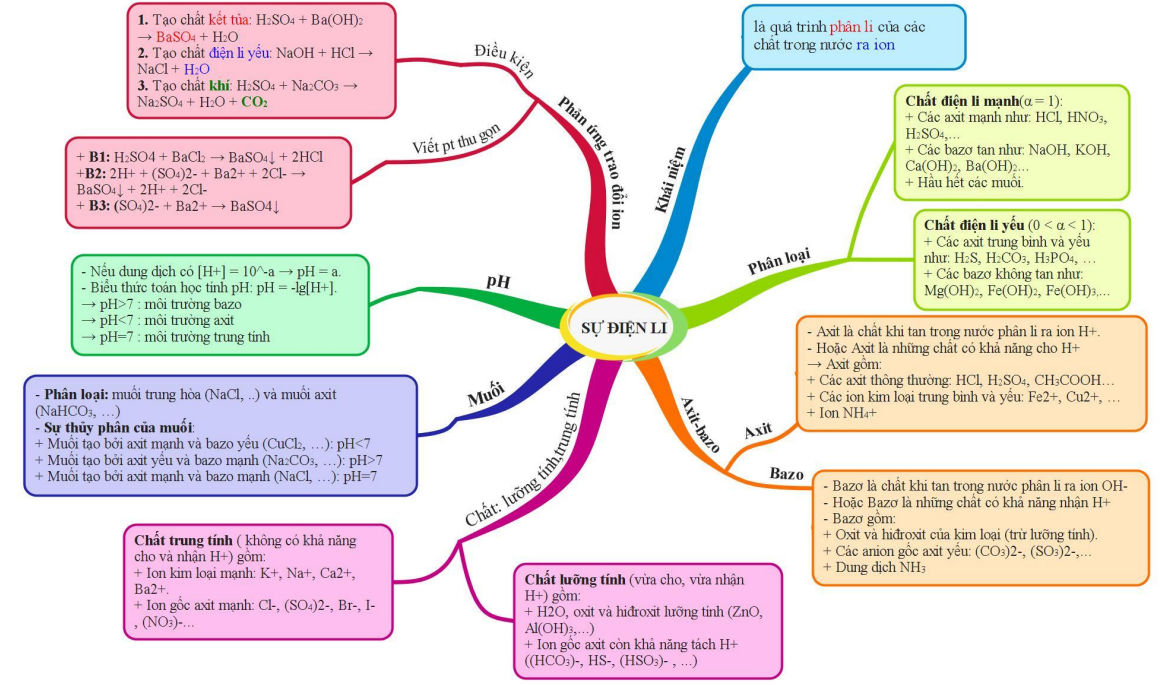
2. Các dạng bài thường gặp
DẠNG 1: BÀI LIÊN QUAN ĐẾN PH CỦA DUNG DỊCH
a) Tính pH của dung dịch (Bài toán xuôi)
– Công thức tính pH của dung dịch: pH= – lg[ H+]
– Cách hỏi 1: Tính pH của dung dịch chứa 1 chất tan.
– Cách hỏi 2: Tính pH của dung dịch chứa 2 chất tan trở lên trong đó các chất không phản ứng với nhau.
– Cách hỏi 3: Tính pH của dung dịch chứa 2 chất tan trở lên trong đó các chất có phản ứng với nhau.
Bước 1: Tính tổng số mol H+
Bước 2: Tính tổng số mol OH
Bước 3: Viết pt ion rút gọn H+ + OH và tính lượng chất dư ⇒ pH của dung dịch.

DẠNG 2: BÀI LIÊN QUAN ĐẾN PHƯƠNG PHÁP BẢO TOÀN ĐIỆN TÍCH
– Trong dung dịch chứa các chất điện li, tổng số mol điện tích dương và âm luôn luôn bằng nhau.

CHƯƠNG 2: NITO – PHOTPHO
1. Nito và hợp chất
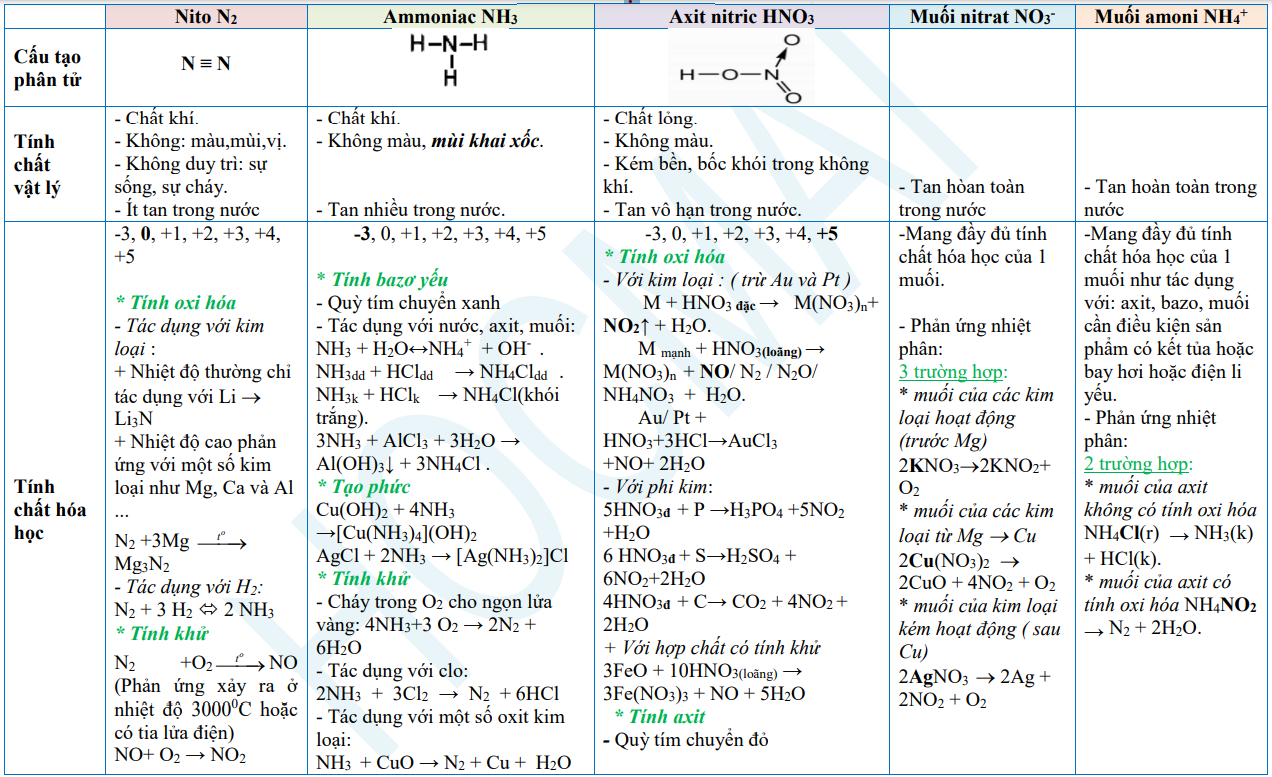
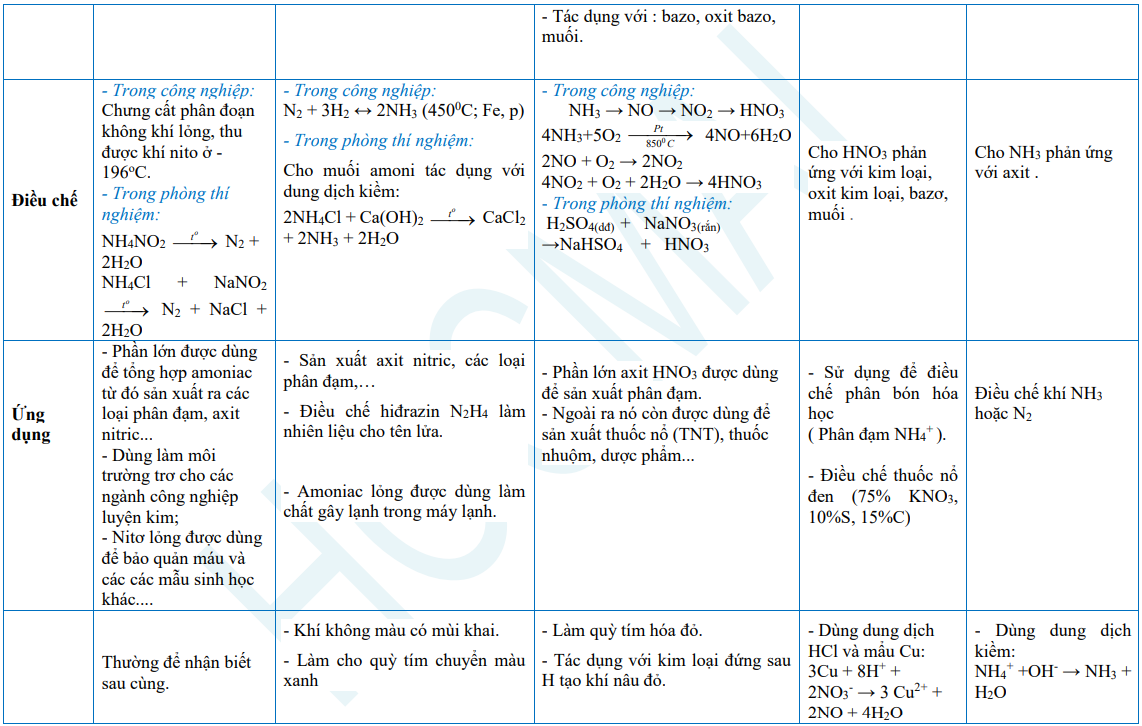

2. Photpho và hợp chất
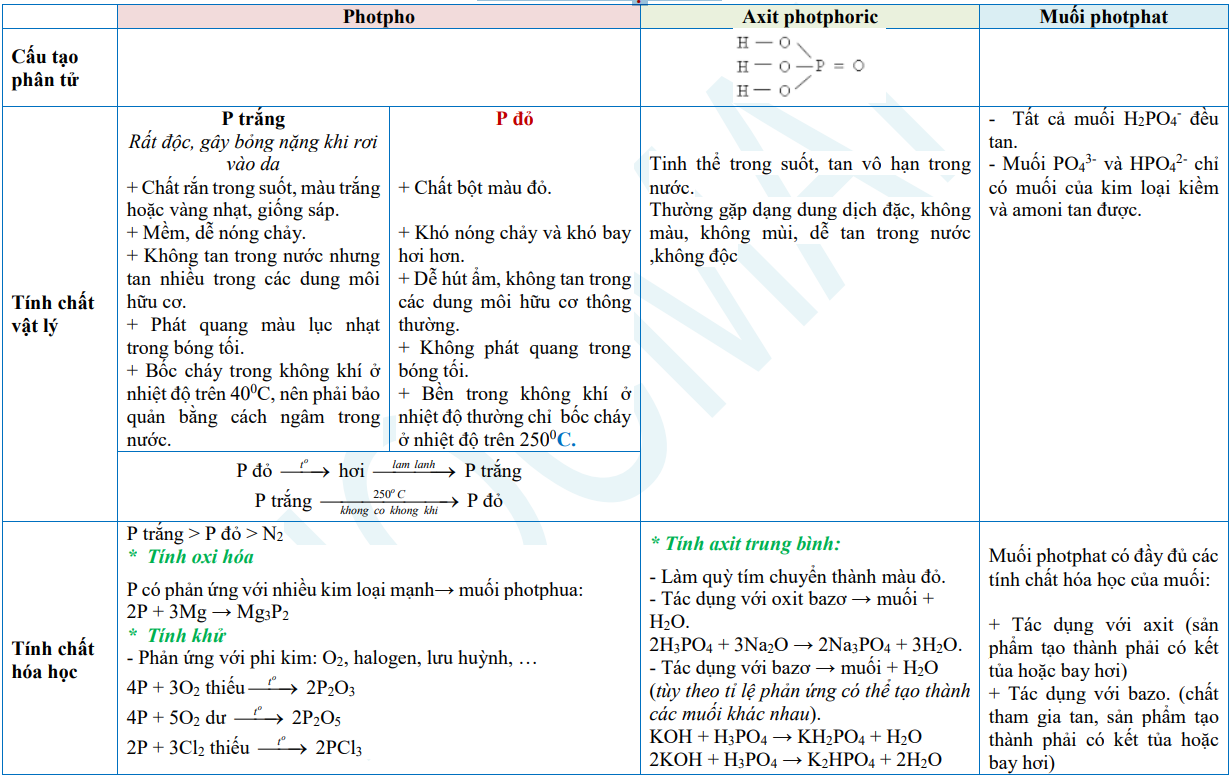
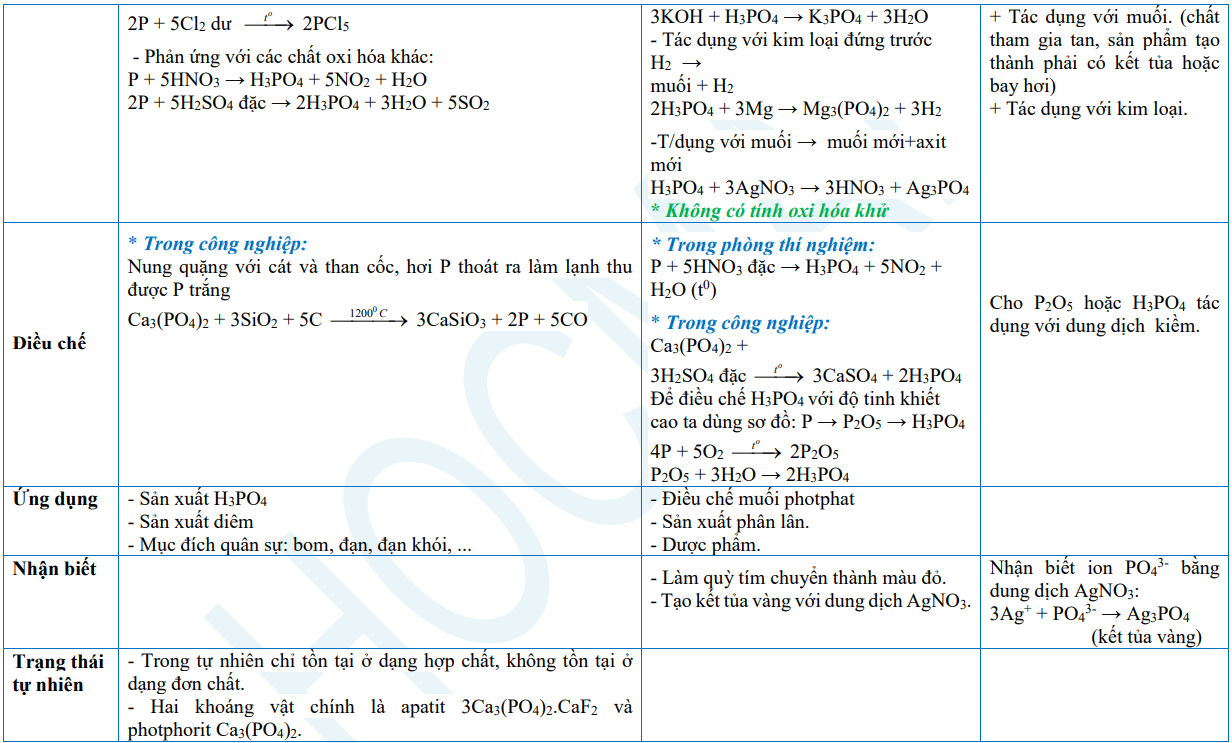
3. Phân bón hóa học
Phân bón hóa học là những hóa chất có chứa các nguyên tố dinh dưỡng, được bón cho cây nhằm tăng năng suất cây trồng.
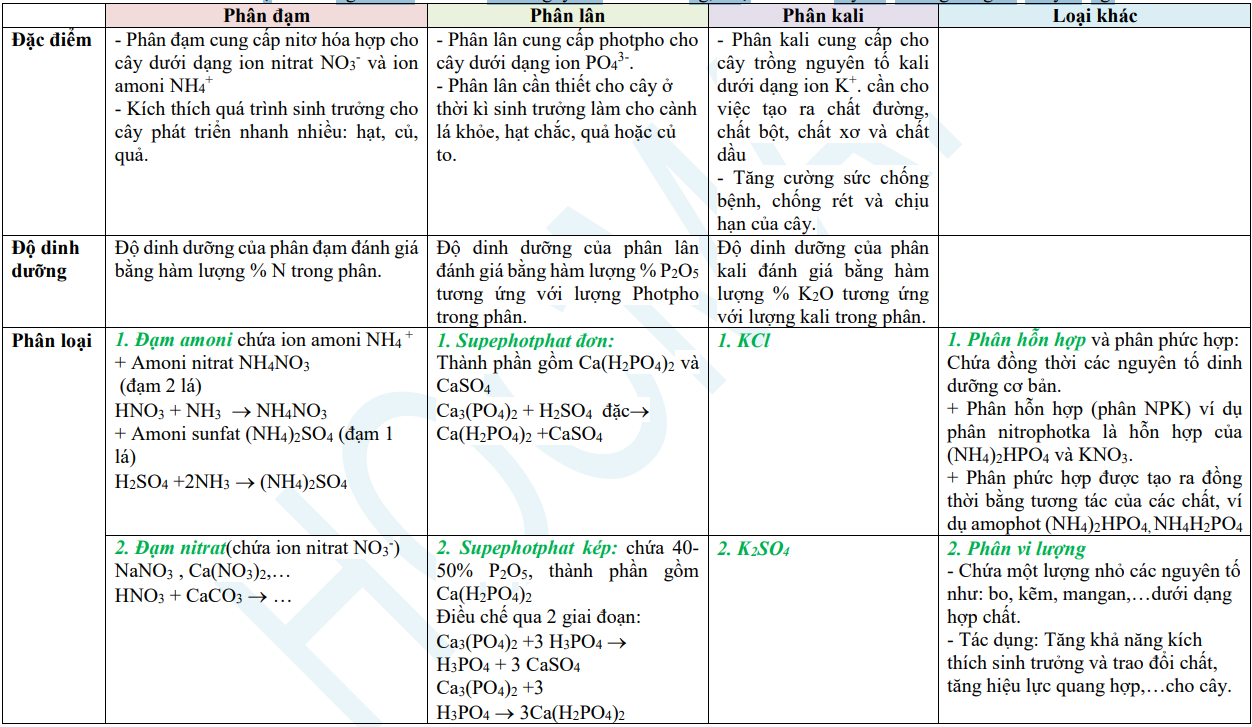

4. Các dạng bài thường gặp
DẠNG BÀI LIÊN QUAN ĐẾN AMONIAC

DẠNG BÀI LIÊN QUAN ĐẾN AXIT NITRIC
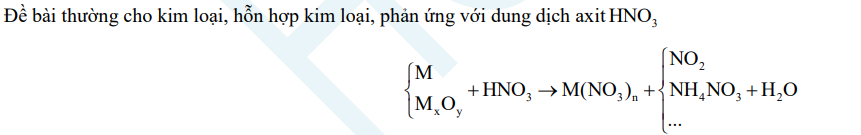

DẠNG BÀI LIÊN QUAN ĐẾN H3PO4 PHẢN ỨNG VỚI DUNG DỊCH BAZƠ

CHƯƠNG 3: CACBON – SILIC
1. Lý thuyết trọng tâm
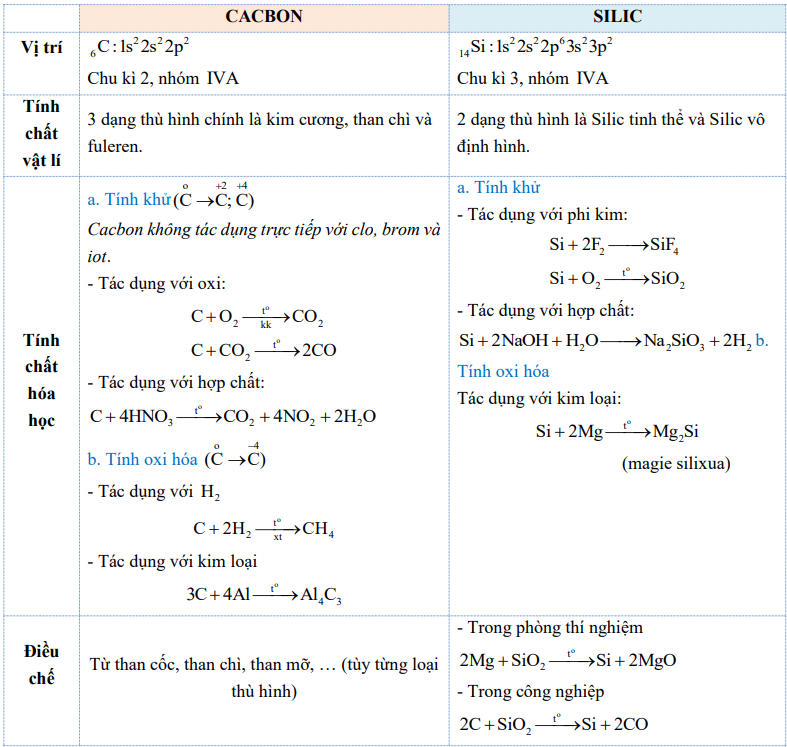

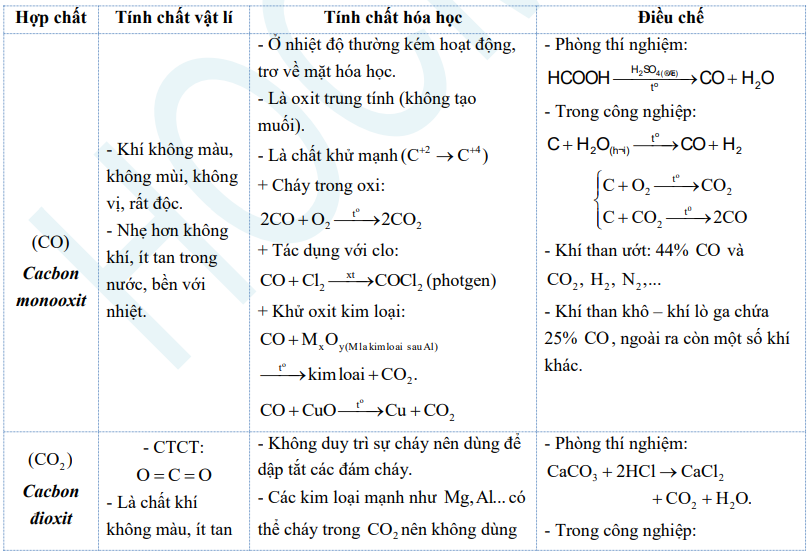


2. Các dạng bài thường gặp
Dạng 1: Bài toán CO khử oxit kim loại

Dạng 2: Bài toán CO2 tác dụng với dung dịch kiềm

⇒ m dung dịch giảm = mCaCO3 – mCO2 = 10 – 0,2. 44 = 1,2 gam.
Dạng 3: Bài toán muối cacbonat tác dụng với dung dịch axit dư

Dạng 5: Bài toán đổ từ từ axit vào muối cacbonat và ngược lại

Dạng 6: Bài toán nhiệt phân muối cacbonat
+ Các muối CO3 2- của kim loại kiềm rất bền với nhiệt.

CHƯƠNG 4: ĐẠI CƯƠNG HÓA HỮU CƠ
1. Khái niệm hợp chất hữu cơ và hoá học hữu cơ
– Hợp chất hữu cơ là các hợp chất của C trừ oxit của C, muối cacbua, muối cacbonat, muối xianua.
– Hoá học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
2. Đặc điểm của hợp chất hữu cơ
– Hợp chất hữu cơ nhất thiết phải chứa C, hay có H thường gặp O ngoài ra còn có halogen, N, P…
– Liên kết chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
– Các hợp chất hữu cơ thường dễ bay hơi, dễ cháy, kém bền nhiệt.
– Các phản ứng trong hoá học hữu cơ thường chậm, không hoàn toàn, xảy ra theo nhiều hướng thường phải đun nóng và có xúc tác.
3. Các phương pháp tinh chế hợp chất hữu cơ
– Chưng cất: để tách các chất lỏng có nhiệt độ sôi khác nhau nhiều.
– Chiết: để tách hai chất lỏng không trộn lẫn vào nhau.
– Kết tinh lại: để tách các chất rắn có độ tan khác nhau theo nhiệt độ.
4. Đồng đẳng và đồng phân
a) Đồng đẳng
– Đồng đẳng là hiện tượng các chất hữu cơ có cấu tạo và tính chất hóa học tương tự nhau nhưng thành phần phân tử khác nhau một hay nhiều nhóm CH2.
– Các chất thuộc cùng dãy đồng đẳng hợp thành một dãy đồng đẳng có công thức chung.
b) Đồng phân
– Đồng phân là các chất hữu cơ có cùng công thức phân tử nhưng cấu tạo khác nhau nên tính chất hóa học khác nhau.
– Có 2 loại đồng phân: Đồng phân cấu tạo và đồng phân lập thể (đồng phân cis – trans).
5. Các loại công thức của hợp chất hữu cơ
– Công thức tổng quát là công thức cho biết hợp chất hữu cơ chứa nguyên tử của những nguyên tố nào.
Ví dụ: CxHy
– Công thức đơn giản nhất là công thức cho biết tỷ lệ tối giản số nguyên tử mỗi nguyên tố trong hợp chất hữu cơ.
Ví dụ: CH2
– Công thức phân tử là công thức cho biết số nguyên tử mỗi nguyên tố có trong hợp chất hữu cơ.
Ví dụ: C2H4
– Công thức cấu tạo là công thức cho biết thứ tự liên kết và kiểu liên kết giữa các nguyên tử trong hợp chất hữu cơ.
Ví dụ: CH2=CH2
6. Dạng bài thường gặp
Dạng 1: Xác định số đồng phân của hợp chất hữu cơ

Dạng 2: Xác định công thức của hợp chất hữu cơ

B – ĐỀ ÔN THI HỌC KÌ 1 MÔN HÓA 11 THEO CHƯƠNG TRÌNH MỚI
Sau khi ôn luyện lại toàn những bộ kiến thức lý thuyết đã được học trong chương trình bộ môn Sinh Học lớp 11, các em hãy luyện tập cùng các đề thi để nắm chắc cũng như làm quen được với ma trận đề thi. Dưới đây là 3 bộ đề thi có kèm lời giải chi tiết, các em học sinh tham khảo ngay tại đây:
Trên đây là Đề cương ôn thi học kì 1 môn Hóa 11 đầy đủ và chi tiết nhất do HOCMAI biên soạn. Hy vọng với những kiến thức trọng tâm, các các dạng bài thường gặp được tổng hợp cũng như các bộ đề thi ôn luyện ở trong bài, các em học sinh khối 11 sẽ nắm chắc kiến thức và chuẩn bị tốt nhất cho kỳ thi cuối học kỳ I sắp tới nhé!


























